Selasa, 27 Maret 2012
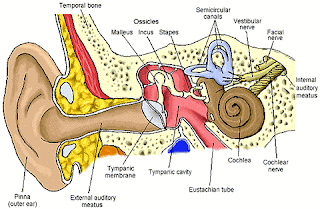
InderaTelinga.ppt
Suara adalah gelombang mekanik (merambat melalui medium) dengan adanya regangan dan kompresi, berasal dari energi kinetik sebagai sumber suara. Partikel dalam medium akan berpindah (gelombang) dan bergerak (osilasi).buat teman teman yang ingin mengetahui tentang suara dalam bidang kesehatan
silahkan klik download disini
InderaMata.ppt
lensa mempunyai fungsi Untuk membentuk bayangan yang tajam atau clear pada layar maka bukaan harus berukuran sangat kecil.
Problems:
Jika bukaan kecil :
Sedikit foton yg dapat masuk
Bayangan gelap
Ratio diameter pinhole dan jarak bayangan harus lebih kecil dari 1/100
Layar bayangan harus besar
Mata harus MASSIVE
Terjadi Diffraction dan and bayangan/membayang (Vignetting)
ini adalah bagian tentang mata. untuk mempelajari lebih lanjut tentang mata
silahkan klik download disini
LOUIS JOSEPH GAY-LUSSAC.ppt
Pada tahun 1808 Joseph Louis Gay-Lussac (1778–1850) berhasil mengukur volume uap air yang terbentuk, sehingga diperoleh perbandingan volume
hidrogen : oksigen : uap air = 2 : 1 : 2,
2H2 (g) + O2 (g) 2H2O(g)
artinya 2 volume gas hidrogen (T0C dan P cm Hg) akan bereaksi dengan 1 volume gas oksigen (T0C dan P cm Hg) untuk menghasilkan air,dengan syarat harus di ukur pada suhu dan tekanan yang sama.
bagaimana tertarik??
silahkan klik download disini
lavoiser.ppt
Ilmuwan Perancis hebat Antoine Laurent Lavoisier merupakan tokoh terkemuka di bidang perkembangan ilmu kimia. Pada saat kelahirannya di Paris tahun 1743, ilmu pengetahuan kimia ketinggalan jauh ketimbang fisika, matematika dan astronomi. Sejumlah besar penemuan yang berdiri sendiri-sendiri sudah banyak diketemukan oleh para ahli ilmu kimia, tetapi tak satu pun kerangka teori yang dapat jadi pegangan yang dapat merangkum informasi yang terpisah-pisah. Pada saat itu tersebar semacam kepercayaan yang tak meyakinkan bahwa air dan udara merupakan substansi yang elementer. Lebih buruk lagi, adanya kesalahfahaman mengenai hakekat daripada api. Kepercayaan yang berkembang saat itu adalah bahwa semua proses pembakaran benda mengandung substansi duga-dugaan yang disebut “phlogiston,” dan bahwa selama proses pembakaran, substansi barang yang terbakar melepaskan phlogiston-nya ke udara.
Dalam jangka waktu antara tahun 1754 – 1774, ahli-ahli kimia berbakat seperti Joseph Black, Joseph Priestley, Henry Cavendish dan lain-lainnya telah mengisolir arti penting gas seperti oxygen, hydrogen, nitrogen dan carbon dioxide. Tetapi, sejak orang-orang ini menerima teori phlogiston, mereka tidak mau memahami hakikat atau arti penting substansi kimiawi yang telah mereka ketemukan. Oxygen, misalnya, dipandang sebagai udara yang semua phlogiston-nya telah dialihkan. (Sebagaimana diketahui bahwa serpihan kayu lebih sempurna terbakar dalam oxygen ketimbang dalam udara; mungkin ini akibat udara lebih mudah menghisap phlogiston dari kayu yang terbaru). Jelas, kemajuan nyata di bidang kimia tidak bisa terjadi sebelum dasar-dasar utamanya dapat difahami.
Adapun Lavoisier yang berhasil dan menangani bagian-bagian yang menjadi teka-teki menjadi satu kesatuan yang dapat dibenarkan dan menemukan arah yang tepat dalam teori ilmu kimia. Pada tahap pertama, kata Lavoisier, teori phlogiston sepenuhnya meleset: tidak ada benda yang namanya phlogiston. Proses pembakaran terdiri dari kombinasi kimiawi tentang terbakarnya barang dengan oxygen. Kedua, air bukanlah barang elementer samasekali melainkan satu campuran antara oxygen dan hydrogen. Udara bukanlah juga substansi elementer melainkan terdiri terutama dari campuran dua jenis gas, oxygen dan nitrogen. Semua pernyataan ini kini tampak gamblang sekarang, tetapi belum bisa ditangkap baik oleh pendahulu-pendahulu Lavoisier maupun rekan sejamannya. Bahkan sesudah Lavoisier merumuskan teorinya dan mengajukan kepada kalangan ilmuwan, toh masih banyak juga pemuka-pemuka ahli kimia yang menolak gagasan teori ini. Tetapi, buku Lavoisier yang brilian Pokok-pokok Dasar Kimia (1789), begitu terang dan jernihnya mengedepankan hipotesa ini dan begitu meyakinkan serta mengungguli pendapat-pendapat lain, barulah ahli-ahli kimia angkatan lebih muda dengan cepat mempercayainya.Seraya membuktikan bahwa air dan udara bukanlah unsur kimiawi, Lavoisier mencantumkan pula dalam bukunya daftar substansi benda-benda itu yang dianggapnya punya arti mendasar dan bersifat elementer meski daftarnya mengandung beberapa kekeliruan, daftar unsur kimiawi modern sekarang ini pada hakekatnya merupakan perluasan dari apa yang sudah disusun Lavoiser itu.Lavoiser sudah menyusun skema pertama yang tersusun rapi tentang sistem kimiawi (bekerja sama dengan Berthollet, Fourcroi dan Guyton de Morveau). Dalam sistem Lavoisier (yang jadi dasar pegangan hingga sekarang) komposisi kimia dilukiskan dengan namanya. Untuk pertama kalinya penerimaan suatu sistem kimia yang seragam dijabarkan sehingga memungkinkan para ahli kimia di seluruh dunia dapat saling berhubungan satu sama lain dalam hal penemuan-penemuan mereka.
Dari hasil eksperimen yang telah dilakukan, Lavoiser dapat merumuskan hukum dasar kimia yaitu hukum kekekalan massa yang berbunyi: ”Dalam suatu reaksi, massa zat sebelum dan sesudah reaksi adalah sama”, dengan kata lain massa tidak dapat diciptakan dan tidak dapat dimusnahkan. Artinya selama reaksi terjadi tidak ada atom-atom pereaksi dan hasil reaksi yang hilang.Pernyataan yang umum untuk menyatakan hukum kekekalan massa adalah massa dapat berubah bentuk tetapi tidak dapat diciptakan atau dimusnahkan. Untuk suatu proses kimiawi di dalam suatu sistem tertutup, massa dari reaktan harus sama dengan massa produk.Hukum kekekalan massa digunakan secara luas dalam bidang-bidang seperti kimia, teknik kimia, mekanika, dan dinamika fluida.
untuk mengetahui lebih lanjut tentang dia
silahkan klik download disini
JONS JACOB BERZELIUS.ppt
“Semua molekul diikat oleh Gaya Coulomb, sehingga gaya tarik elektrostatis antar benda bermuatan berbeda yaitu positif atau negatif dan dalam jumlah berbeda”
Menurut aksioma Berzelius, atom hidrogen bermuatan positif dan atom khlorin bersifat negatif. Menurut teori Berzelius, walaupun asam asetat, CH3COOH, bersifat asam, asam trikhloroasetat, CCl3COOH, seharusnya basa. Berzelius percaya bahwa muatan listrik adalah asal usul keasaman dan kebasaan. Karena penukaran hidrogen dengan khlorin, yang muatannya berlawanan, akan membentuk basa. Faktanya asam trikhloroasetat asam, bahkan lebih asam dari asam asetat Dualisme elektrokimia dengan demikian perlahan ditinggalkan.
banyak hal yang dianggap berbeda silahkan baca lebih lanjut.
silahkan klik download disini
JOSEPH PRISTLEY.ppt
Joseph Priestley dikenal sebagai raja penemu gas. Seolah tidak puas dengan penemuan gas bersoda dan gas ketawa, Pristley melakukan eksperimen dengan memanaskan calx merkuri (merkuri oksida) yang berupa serbuk merah. Dari eksperimen tersebut beliau menemukan oksigen pada tahun 1774. Priestley menamai gas yang ditemukannya sebagai ‘de-phlogisticated air’ sesuai dengan petunjuk teori phlogiston yang saat itu dipercaya.
untuk mendownload file ini
silahkan klik download disini
Johann Wolfgang Dobereiner.ppt
Johan Wolfgang Dobreiner (13 Desember 1780 - 24 Maret ) adalah seorang ahli kimia Jerman yang terkenal karena pekerjaan yang meramalkan hukum periodik untuk unsur kimia.
Dobreiner adalah anak dari Johann Adam Dobreiner seorang pekarja peternakan yang bangkit untuk menjadi seorang manajer perkebunan dan Johanna Susanna Goring. Pada tahun 1784 ia magang di apotek yang bernama Lutz.
Dobreiner memiliki kesempatan untuk sekolah formal dan magang untuk apotek membaca secara luas dan menghadiri kuliah sains. Dia akhirnya menjadi profesor kimia dan farmasi di Universitas Jena pada bulan Agustus 1810 dan juga memungkinkan mendapatkan gelar Doktor pada bulan november pada tahun itu juga.
Pada tahun 1812 Dobhreiner terlibat dalam konversi pati menjadi gula. Dia juga memberikaian kuliah pada kimia praktis untuk sekelompok teknisi dan mengajar mata kuliah khusus untuk para ekonom dan administrator. Dobreiner juga melakukan penelitian lebih lanjut dengan platinum spons, yang disiapkan dengan membusukkan garam platinum ke dalam larutan dan langsung memanaskannya.
Selain karyanya dengan oksida dan platinum garam kompleks , ia juga menyelidiki suatu zat yang terbentuk dari logam yang disebut Liebig dipelajari “platina hitam”. Peran bahan ini dalam proses oksidasi sulfur dioksida dan alkohol, dan disusulkan penggunaannya untuk memproduksi asam asetat dari bahan yang ke dua. Ia membusukkan paduan platina baku hitam dengan asam encer dan menemukan bubuk hitam yang terkandung platinum, palladium, iridium, rutenium dan osmium. Ini dapat meledak di pancuran bunga api ketika dibawa kontak langsung dengan udara.
untuk mendownload file
silahkan klik download disini
HENRY CAVENDISH AND THE HYDROGEN.ppt
Henry Cavendish lahir pada 10 Oktober 1731 anak sulung Charles dan Lady Anne Cavendish Grey. Ia masuk Peterhouse, Cambridge, pada 1749 dan meninggalkannya setelah 2 tahun tanpa gelar. Dia tidak pernah menikah dan begitu diketahui bahwa ada catatan kecil yang memiliki kehidupan sosial kecuali ada pertemuan sesekali dengan teman-teman ilmiah. Kematiannya (24 Februari 1810) dan dimakamkan di Gereja Saints Semua, Derby.
Cavendish kerja dan reputasi harus dipertimbangkan dalam dua bagian: satu berhubungan dengan karyanya yang diterbitkan, yang lain dengan jumlah besar tidak ia publikasikan. Selama hidupnya ia membuat penemuan penting dalam kimia terutama antara 1766 dan 1788 dan dalam listrik antara 1771 dan 1788. Pada 1798 ia menerbitkan sebuah makalah penting tunggal pada kepadatan bumi, namun minat pada pelajaran ini jelas berlangsung lama.
bagaimana? ingin tahu lebih lanjut ?
silahkan klik download disini
Atom Dalton.ppt
Salah satu konsep ilmiah tertua adalah bahwa semua materi dapat dipecah menjadi zarah (partikel) terkecil , dimana partikel – partikel ini tidak dapat bias dibagi lebih lanjut. Filosof Yunani Democritus (kira – kira 460 – 370 SM ) menyatakan bahwa partikel ini berada pada gerakan yang konstan, tetapi dapat bergabung membentuk suatu kombinasi yang mantap. Menurut dugaan , sifat – sifat tertentu dari suatu bahan diakibatkan oleh perbedaan ukuran , bentuk , dan susunan partikel – partikelnya. Sekarang, partikel – partikel kecil ini yang menyusun semua materi dinamakan atom. [atomos (a, tidak + tomos, memotong ) – tidak terpotong , tidak dapat dibagi]. Banyak ilmuwan yang kemudian menemukan lebih banyak mengenai sifat – sifat atom berdasar percobaan.
Namun pendapat Democritus tidak disertai bukti ilmiah melalui experiment. Dengan makin berkembangnya teknologi,maka muncul beberapa teori tentang atom.Salah satu teori dikemukakan oleh John Dalton. Sumbangan Dalton merupakan keunikan dari teorinya yang meliputi dua hal : Dia adalah orang pertama yang melibatkan kejadian kimiawi seperti halnya kejadian fisis dalam merumuskan gagasannya tentang atom. Juga mendasarkan asumsinya pada data kuantitatif, tidak menggunakan pengamatan kualitatif atau untung – untungan.
untuk tahu lebih lanjut
silahkan klik download disini
NEWSLANDS.ppt
Pada tahun 1865, John Newlands menemukan hubungan lain antara massa atom relatif suatu unsur dengan sifat unsur tersebut. Ia menyusun unsur dalam tujuh kelompok unsur, dan setiap unsur kedelapan mempunyai sifat yang sama seperti sifat unsur pertama (seperti oktaf dalam nada musik), yang disebut dengan hukum oktaf.[1]
Meskipun ada hal yang tidak dapat diterima (misalnya Cr tidak mirip dengan Al, Mn tidak mirip dengan P, Fe tidak mirip dengan S, dan lain-lain), tetapi usahanya telah menuju ke arah yang lebih tepat dalam menyusuf daftar-daftar unsur.[1]
untuk tahu lebih lanjut silahkan download
silahkan klik download disini
Metode Secant.ppt
Tentukan X0, X1, toleransi, dan jumlah iterasi maksimum.
Hitung Xbaru = X1 - f(X1)( X1- X0)/f(X1) – f(X0).
Jika nilai mutlak (Xbaru - X1) < toleransi, diperoleh tulisan xbaru sebagai hasil perhitungan.
jika tidak, lanjutkan ke langkah berikutnya.
Jika jumlah iterasi > iterasi maksimum, akhiri program.
X = Xbaru, dan kembali ke langkah (2).
diatas adalah alogaritma metode ini. ingin tahu lebih lanjut silahkan didownload
silahkan klik download disini
MetodeIterasiSatuTitikSederhana.ppt
Metode Iterasi Titik tetap kadang-kadang dinamakan metode iterasi sederhana atau metode langsung atau metode substitusi beruntun. Kesederhanaan metode ini karena pembentukan prosedur iterasinya yang mudah dibentuk, yaitu kita ubah persamaan f (x) = 0 menjadi bentuk x = g(x), kemudian dibentuk menjadi prosedur iterasi,
Metode iterasi sederhana adalah metode yang memisahkan x dengan sebagian x yang lain sehingga diperoleh : x = g(x).
dikenal juga sebagai metode x = g(x)
Bentuk iterasi satu titik ini dapat dituliskan dalam bentuk
x(n+1)=g(xn)
Dimana n=0,1,2,3,....
untuk mempelajari lebih lanjut silahkan didownload filenya
silahkan klik download disini
MetodeNewton-Raphson.ppt
Kelemahan
Metode Newton-Raphson
1. Jika fungsi f(x) mempunyai beberapa akar (titik) penyelesaian, akar-akar penyelesaian tersebut tidak dapat dicari secara bersamaan.
2. Tidak dapat mencari akar kompleks (imajiner).
3. Tidak bisa mencari akar persamaan yang tidak memenuhi persyaratan persamaannya, meskipun ada akar penyelesaiannya.
4. Untuk persamaan non linier yang cukup kompleks, pencarian turunan pertama dan kedua f(x) akan menjadi sulit.
hal diatas merupakan kelemahan dari metode ini untuk mengetahui lebih lanjut silahkan download aja filenya.
silahkan klik download disini
kuliahkomputasi1.ppt
Langkah 1 : Pilih taksiran nilai x1 sebagai batas bawah interval dan taksiran nilai x2 sebagai batas atas interval.
Jika terpenuhi kondisi :
f(x1) x f(x2) < 0 maka ada akar dalam interval. Selanjutnya ke langkah 2.
f(x1) x f(x2) > 0 maka tidak ada akar dalam interval. Geser posisi interval.
f(x1) x f(x2) = 0 maka xl atau xu , salah satu merupakan akar.
hal diatas adalah langkah pertama dari metode bisection, untuk tahu tentang metode dasar ini silahkan download filenya.
silahkan klik download disini
FalsePositionMethod.ppt
The false-position method is a modification on the bisection method: if it is known that the root lies on [a, b], then it is reasonable that we can approximate the function on the interval by interpolating the points (a, f(a)) and (b, f(b)). In that case, why not use the root of this linear interpolation as our next approximation to the root?
untuk mengetahui tentang metode ini silahkan download filenya
FalsePositionMethod
silahkan klik download disini
Langganan:
Komentar (Atom)